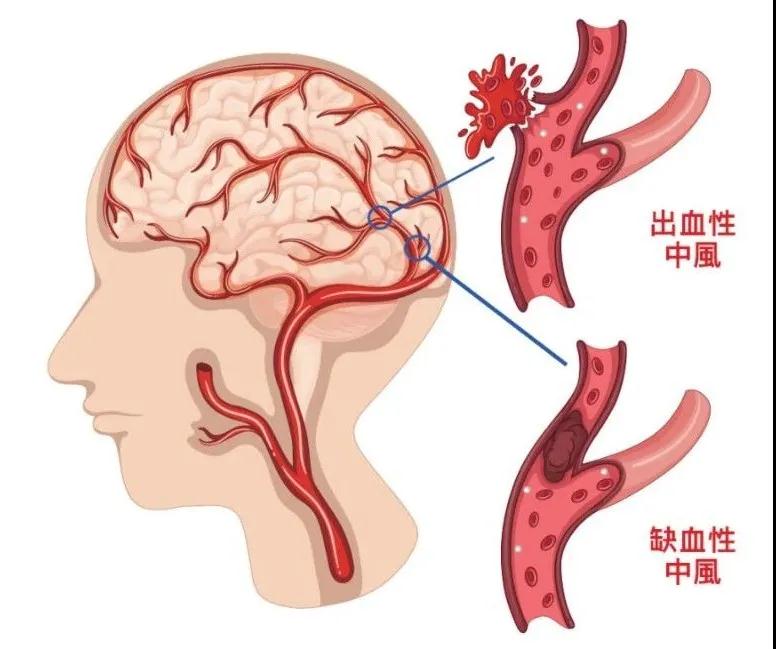
中风是一组以脑部缺血和出血性损伤为临床表现的一种疾病,具有极高的死亡率和致残率。缺血性中风约占所有中风的85%,其余为出血性中风。缺血性中风是全球一个重大的健康问题,随着人口老龄化,中风的发生率可能还将持续增加。
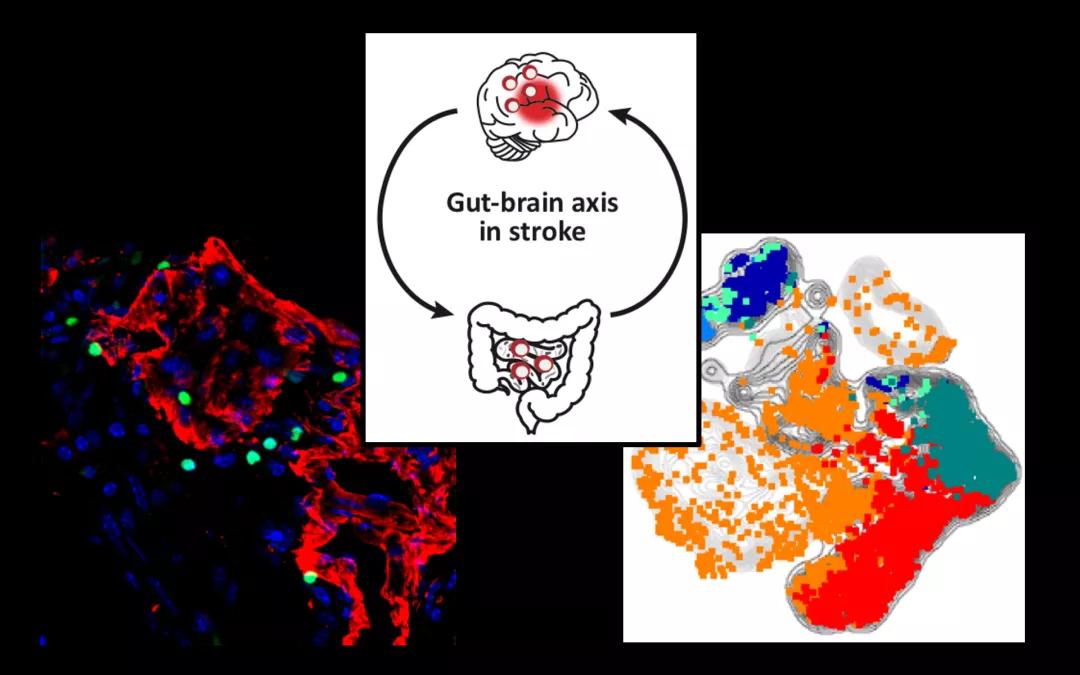
近年来,肠道菌群在疾病发病机制中的作用以及改变肠道菌群对疾病的治疗潜力,引起了越来越多的关注。肠道菌群在维持宿主健康中发挥着重要作用。相当比例的中风患者患有胃肠道并发症,包括吞咽困难、胃肠出血和便秘,这些并发症通常会对中风结果产生不利影响。越来越多的研究发现,肠道菌群和大脑之间的相互作用在中风的发生以及中风的结果中发挥重要作用。
肠道菌群如何增加中风风险?
氧化三甲胺是肠道微生物的代谢物之一,也是研究得最透彻的肠道菌群与中风风险之间的联系之一。早期的动物研究表明,富含磷脂酰胆碱的饮食(比如红肉)会促进动脉粥样硬化的发生,而肠道菌群对磷脂酰胆碱的代谢在其中发挥重要作用。肠道微生物会代谢膳食中的磷脂酰胆碱,首先形成三甲胺,然后三甲胺会被肝脏中的黄素单加氧酶转化为氧化三甲胺。
一项大型临床研究对4000多名选择性冠状动脉造影患者进行了3年的随访研究,评估了这期间空腹血浆氧化三甲胺水平与主要不良心血管事件(死亡、心肌梗死或中风)之间的关系。结果发现,膳食中磷脂酰胆碱产生的氧化三甲胺依赖于肠道菌群的代谢,氧化三甲胺水平的升高与主要不良心血管事件的风险增加有关。这种联系在其它研究中也得到了证实。
一项针对我国高血压患者的嵌套病例对照研究显示,较高的氧化三甲胺水平与初发脑中风风险增加有关。另一项对接受了颈动脉支架植入手术的颈动脉严重狭窄患者的研究报道,支架植入后,氧化三甲胺水平的增加与新的脑缺血性损伤的风险增加有关。
氧化三甲胺、动脉粥样硬化和中风风险之间的关系似乎已得到很好的证实,那么,氧化三甲胺是如何调节动脉粥样硬化风险的呢?
1)氧化三甲胺增加心血管疾病和动脉粥样硬化风险的一种可能的机制是氧化三甲胺介导的促炎单核细胞和血管炎症的增加,在缺血性中风患者中也是如此,氧化三甲胺水平升高与复发性中风风险呈剂量依赖关系。此外,氧化三甲胺水平与促炎症的单核细胞百分比之间也存在显著的相关性。
2)氧化三甲胺的其它机制包括其对血小板高反应性、胆固醇代谢、和泡沫细胞形成(在动脉粥样硬化的发病中起关键作用)的调节作用。
3)此外,血浆氧化三甲胺水平也被证明与缺血性中风的其它危险因素相关,包括房颤和糖尿病,这些因素本身就会导致中风风险的升高。
除氧化三甲胺外,其它研究也表明,根据中风风险不同,患者的肠道菌群也不同。具体来说,在高风险人群中,条件致病菌明显增多,而产丁酸的细菌明显减少。因此,肠道菌群组成的改变可能增加中风的风险。
中风会导致肠道菌群失衡吗?
急性缺血性中风会导致肠道菌群失调,而肠道菌群的变化反过来又会影响神经炎症过程并影响中风的结果。
首先,一些基于动物的研究表明,中风后的动物模型和对照组之间的肠道菌群组成存在显著差异。一项研究显示,局灶性脑缺血导致小鼠中风后,胃肠道各个部分的菌群都发生了实质性的变化,甚至在细菌门水平上也存在差异;而中风引起的肠道黏膜菌群组成变化的主要特征是嗜黏蛋白阿尔曼氏菌丰度增加和梭菌属细菌过量繁殖。
另一项利用大脑中动脉栓塞的小鼠中风模型的研究发现,严重中风3天后,肠道菌群组成发生了明显变化,主要表现为物种多样性降低,拟杆菌门细菌过度生长。
目前,评价中风后肠道菌群变化的临床研究还比较有限。一项研究评估了中风患者的粪便菌群和粪便有机酸,结果发现,与对照组相比,中风患者的瘤胃乳杆菌(Lactobacillus ruminis)数量显著增加;相反,缺血性中风也与其它种类的乳酸杆菌数量减少有关,比如清酒乳杆菌。虽然,不同的研究得到了不太一致的结果,但毫无疑问,中风会改变患者的肠道菌群组成。
那么,中风是如何导致肠道菌群失衡的呢?
一种可能的机制是,急性缺血性脑中风后,由于中风后应激反应导致胃肠道运动降低,从而导致细菌过度生长。比如在动物模型中观察到的物种多样性减少和拟杆菌门细菌过度生长是中风后肠道菌群失调的标志,这就与肠道运动减少相关。
自主神经系统也参与调节中风对肠道菌群失衡的影响。中风会改变盲肠菌群的组成,并根据损伤的严重程度而有不同的变化,这是通过自主神经系统释放的去甲肾上腺素以及盲肠黏液蛋白的产生和杯状细胞数量的改变来调节的。
此外,中风后应激反应会通过释放促肾上腺皮质激素释放激素和糖皮质激素,增加肠道通透性,导致肠道细菌易位增加。这与临床报道的重型颅脑损伤和缺血性中风患者胃肠运动受损和胃肠并发症增加的情况是一致的。
急性中风和肠道菌群失调之间的其它潜在机制联系包括坏死的脑组织释放的直接影响肠道菌群组成的物质,比如,三磷酸腺苷、高迁移率族蛋白B1(HMGB1)、S100蛋白等的释放会影响肠道免疫和菌群组成。
肠道菌群如何影响中风结果?
肠道菌群的变化会影响中风后的神经炎症和影响中风的结果。
研究人员先将从中风小鼠和正常小鼠中获得的肠道微生物移植到无菌小鼠中,然后诱导这些小鼠中风,结果发现,与接受正常小鼠肠道微生物的小鼠相比,接受中风小鼠肠道微生物的小鼠梗死面积明显更大。此外,接受中风小鼠菌群移植的小鼠,其促炎性的T细胞表达更高。在中风后2-3天,来自小鼠肠道的T细胞会转移到大脑,加剧神经损伤。
在另一项动物研究中,在诱导中风前使用广谱抗生素(阿莫西林/克拉维酸)清除肠道微生物,可以产生抗炎症的神经保护作用,可使梗死面积减少60%并保留感觉运动功能。
幼鼠和老龄鼠的肠道菌群组成存在显著差异,老龄鼠的肠道菌群与炎症和肠道通透性增加有关。通过粪菌移植改变幼鼠的肠道菌群,使其与老龄鼠相似,通过大脑中动脉栓塞诱导中风后,小鼠死亡率更高,运动功能受损更严重、促炎细胞因子反应更高。相反,改变老龄鼠的肠道菌群,使其与幼鼠相似,可以提高中风后的存活率和促进恢复。
关于急性缺血性中风后的肠道菌群失调与临床结果的相关性的临床研究还相对较少。日本的一项研究报道了瘤胃乳杆菌的丰度变化与血清IL-6的水平正相关。此外,缺血性中风与粪便戊酸(肠道微生物代谢物)浓度增加有关,而戊酸浓度与高敏C反应蛋白等炎症标志物水平和白细胞计数呈正相关。因此,缺血性中风患者的肠道菌群失衡可能影响宿主的代谢和炎症。
另外,研究人员根据中风后的肠道菌群失调特征定义一个叫做SDI(Stroke Dysbiosis Index)的参数,来定义肠道菌群失调的严重程度,这一参数可以作为严重中风和早期不良后果的独立预测因素。如果将SDI指数较高的患者的粪便细菌移植到无菌小鼠,可以导致更严重的脑损伤和肠道促炎症T细胞的增加。
肠道菌群可以作为中风治疗的一个靶点吗?
肠道菌群与中风的发生和预后的关系,为中风的治疗提供了一个新的潜在靶点。
早期的研究显示,血浆氧化三甲胺的水平在使用广谱抗生素后可以被显著抑制,但是停用抗生素后又会上升,这也限制了其使用,毕竟长期使用抗生素可能会增加其它许多健康风险。
有研究人员开发了一种可以有效抑制肠道微生物依赖性氧化三甲胺产生的抑制剂,可能能够降低血栓形成和中风风险。CutC/D是肠道细菌利用胆碱产生三甲胺的关键酶,在动物模型中,单次口服CutC/D抑制剂可以显著降低血浆TMAO水平达3天,挽救饮食诱导的血小板反应性增强和血栓形成,而且无明显毒性,也不会增加出血风险。
粪菌移植是将健康供体的粪便细菌移植到疾病个体的肠道中,重建患者的肠道菌群而达到治疗疾病的目的。粪菌移植作为一种安全有效的治疗复发性艰难梭菌感染的方法已被广泛应用。在动物实验中,移植正常的粪便菌群可以改善中风的结果。
益生菌能够改善肠道菌群,调节细胞因子的释放,影响神经炎症反应,因此可能是急性中风的另一种治疗策略。动物研究表明,益生菌丁酸梭菌可以减轻脑缺血/再灌注造成的小鼠脑功能损伤。粪菌移植和益生菌干预还缺乏在脑中风患者中的临床研究,值得进一步的研究,它们或可作为降低中风的严重程度和促进中风后康复的有效手段。
饮食是影响肠道菌群组成的主要决定因素。事实上,饮食多样性与氧化三甲胺水平的变化也有关系,大量摄入含有左旋肉碱和磷脂酰胆碱的食物(比如红肉),可以增加肠道微生物产生的氧化三甲胺。高脂饮食会增加人体内氧化三甲胺的浓度,而地中海饮食会降低氧化三甲胺的产生。因此,控制饮食是一种改善中风的有效手段,一方面可以通过降低氧化三甲胺的产生而降低中风的风险,另一方面可以通过改善肠道菌群而改善中风结果和促进康复。
总结
肠道菌群与大脑之间存在着密切的相互作用,由于胃肠道并发症在中风患者中非常常见,所以肠道菌群在中风的发生和预后中的作用也日益受到关注。越来越多的研究发现,肠道菌群的改变可能是急性缺血性中风的一个危险因素,增加中风的发生风险;相反,中风也会导致肠道菌群的进一步紊乱,这可能会增加中风的严重程度,导致严重的胃肠道、肝、肾、心血管损伤,包括多器官功能障碍综合征,同时也会影响脑功能的恢复。改善肠道菌群,可能对于减少中风风险,降低中风后的严重程度以及改善预后具有重要意义。
图片均来自网络
参考文献:

编辑:田力

近年来,肠道菌群在疾病发病机制中的作用以及改变肠道菌群对疾病的治疗潜力,引起了越来越多的关注。肠道菌群在维持宿主健康中发挥着重要作用。相当比例的中风患者患有胃肠道并发症,包括吞咽困难、胃肠出血和便秘,这些并发症通常会对中风结果产生不利影响。越来越多的研究发现,肠道菌群和大脑之间的相互作用在中风的发生以及中风的结果中发挥重要作用。
肠道菌群如何增加中风风险?

氧化三甲胺是肠道微生物的代谢物之一,也是研究得最透彻的肠道菌群与中风风险之间的联系之一。早期的动物研究表明,富含磷脂酰胆碱的饮食(比如红肉)会促进动脉粥样硬化的发生,而肠道菌群对磷脂酰胆碱的代谢在其中发挥重要作用。肠道微生物会代谢膳食中的磷脂酰胆碱,首先形成三甲胺,然后三甲胺会被肝脏中的黄素单加氧酶转化为氧化三甲胺。
一项大型临床研究对4000多名选择性冠状动脉造影患者进行了3年的随访研究,评估了这期间空腹血浆氧化三甲胺水平与主要不良心血管事件(死亡、心肌梗死或中风)之间的关系。结果发现,膳食中磷脂酰胆碱产生的氧化三甲胺依赖于肠道菌群的代谢,氧化三甲胺水平的升高与主要不良心血管事件的风险增加有关。这种联系在其它研究中也得到了证实。
一项针对我国高血压患者的嵌套病例对照研究显示,较高的氧化三甲胺水平与初发脑中风风险增加有关。另一项对接受了颈动脉支架植入手术的颈动脉严重狭窄患者的研究报道,支架植入后,氧化三甲胺水平的增加与新的脑缺血性损伤的风险增加有关。
氧化三甲胺、动脉粥样硬化和中风风险之间的关系似乎已得到很好的证实,那么,氧化三甲胺是如何调节动脉粥样硬化风险的呢?
1)氧化三甲胺增加心血管疾病和动脉粥样硬化风险的一种可能的机制是氧化三甲胺介导的促炎单核细胞和血管炎症的增加,在缺血性中风患者中也是如此,氧化三甲胺水平升高与复发性中风风险呈剂量依赖关系。此外,氧化三甲胺水平与促炎症的单核细胞百分比之间也存在显著的相关性。
2)氧化三甲胺的其它机制包括其对血小板高反应性、胆固醇代谢、和泡沫细胞形成(在动脉粥样硬化的发病中起关键作用)的调节作用。
3)此外,血浆氧化三甲胺水平也被证明与缺血性中风的其它危险因素相关,包括房颤和糖尿病,这些因素本身就会导致中风风险的升高。
除氧化三甲胺外,其它研究也表明,根据中风风险不同,患者的肠道菌群也不同。具体来说,在高风险人群中,条件致病菌明显增多,而产丁酸的细菌明显减少。因此,肠道菌群组成的改变可能增加中风的风险。
中风会导致肠道菌群失衡吗?
急性缺血性中风会导致肠道菌群失调,而肠道菌群的变化反过来又会影响神经炎症过程并影响中风的结果。
首先,一些基于动物的研究表明,中风后的动物模型和对照组之间的肠道菌群组成存在显著差异。一项研究显示,局灶性脑缺血导致小鼠中风后,胃肠道各个部分的菌群都发生了实质性的变化,甚至在细菌门水平上也存在差异;而中风引起的肠道黏膜菌群组成变化的主要特征是嗜黏蛋白阿尔曼氏菌丰度增加和梭菌属细菌过量繁殖。
另一项利用大脑中动脉栓塞的小鼠中风模型的研究发现,严重中风3天后,肠道菌群组成发生了明显变化,主要表现为物种多样性降低,拟杆菌门细菌过度生长。
目前,评价中风后肠道菌群变化的临床研究还比较有限。一项研究评估了中风患者的粪便菌群和粪便有机酸,结果发现,与对照组相比,中风患者的瘤胃乳杆菌(Lactobacillus ruminis)数量显著增加;相反,缺血性中风也与其它种类的乳酸杆菌数量减少有关,比如清酒乳杆菌。虽然,不同的研究得到了不太一致的结果,但毫无疑问,中风会改变患者的肠道菌群组成。
那么,中风是如何导致肠道菌群失衡的呢?
一种可能的机制是,急性缺血性脑中风后,由于中风后应激反应导致胃肠道运动降低,从而导致细菌过度生长。比如在动物模型中观察到的物种多样性减少和拟杆菌门细菌过度生长是中风后肠道菌群失调的标志,这就与肠道运动减少相关。
自主神经系统也参与调节中风对肠道菌群失衡的影响。中风会改变盲肠菌群的组成,并根据损伤的严重程度而有不同的变化,这是通过自主神经系统释放的去甲肾上腺素以及盲肠黏液蛋白的产生和杯状细胞数量的改变来调节的。
此外,中风后应激反应会通过释放促肾上腺皮质激素释放激素和糖皮质激素,增加肠道通透性,导致肠道细菌易位增加。这与临床报道的重型颅脑损伤和缺血性中风患者胃肠运动受损和胃肠并发症增加的情况是一致的。
急性中风和肠道菌群失调之间的其它潜在机制联系包括坏死的脑组织释放的直接影响肠道菌群组成的物质,比如,三磷酸腺苷、高迁移率族蛋白B1(HMGB1)、S100蛋白等的释放会影响肠道免疫和菌群组成。

肠道菌群如何影响中风结果?
肠道菌群的变化会影响中风后的神经炎症和影响中风的结果。
研究人员先将从中风小鼠和正常小鼠中获得的肠道微生物移植到无菌小鼠中,然后诱导这些小鼠中风,结果发现,与接受正常小鼠肠道微生物的小鼠相比,接受中风小鼠肠道微生物的小鼠梗死面积明显更大。此外,接受中风小鼠菌群移植的小鼠,其促炎性的T细胞表达更高。在中风后2-3天,来自小鼠肠道的T细胞会转移到大脑,加剧神经损伤。
在另一项动物研究中,在诱导中风前使用广谱抗生素(阿莫西林/克拉维酸)清除肠道微生物,可以产生抗炎症的神经保护作用,可使梗死面积减少60%并保留感觉运动功能。
幼鼠和老龄鼠的肠道菌群组成存在显著差异,老龄鼠的肠道菌群与炎症和肠道通透性增加有关。通过粪菌移植改变幼鼠的肠道菌群,使其与老龄鼠相似,通过大脑中动脉栓塞诱导中风后,小鼠死亡率更高,运动功能受损更严重、促炎细胞因子反应更高。相反,改变老龄鼠的肠道菌群,使其与幼鼠相似,可以提高中风后的存活率和促进恢复。
关于急性缺血性中风后的肠道菌群失调与临床结果的相关性的临床研究还相对较少。日本的一项研究报道了瘤胃乳杆菌的丰度变化与血清IL-6的水平正相关。此外,缺血性中风与粪便戊酸(肠道微生物代谢物)浓度增加有关,而戊酸浓度与高敏C反应蛋白等炎症标志物水平和白细胞计数呈正相关。因此,缺血性中风患者的肠道菌群失衡可能影响宿主的代谢和炎症。
另外,研究人员根据中风后的肠道菌群失调特征定义一个叫做SDI(Stroke Dysbiosis Index)的参数,来定义肠道菌群失调的严重程度,这一参数可以作为严重中风和早期不良后果的独立预测因素。如果将SDI指数较高的患者的粪便细菌移植到无菌小鼠,可以导致更严重的脑损伤和肠道促炎症T细胞的增加。

肠道菌群可以作为中风治疗的一个靶点吗?
肠道菌群与中风的发生和预后的关系,为中风的治疗提供了一个新的潜在靶点。
早期的研究显示,血浆氧化三甲胺的水平在使用广谱抗生素后可以被显著抑制,但是停用抗生素后又会上升,这也限制了其使用,毕竟长期使用抗生素可能会增加其它许多健康风险。
有研究人员开发了一种可以有效抑制肠道微生物依赖性氧化三甲胺产生的抑制剂,可能能够降低血栓形成和中风风险。CutC/D是肠道细菌利用胆碱产生三甲胺的关键酶,在动物模型中,单次口服CutC/D抑制剂可以显著降低血浆TMAO水平达3天,挽救饮食诱导的血小板反应性增强和血栓形成,而且无明显毒性,也不会增加出血风险。
粪菌移植是将健康供体的粪便细菌移植到疾病个体的肠道中,重建患者的肠道菌群而达到治疗疾病的目的。粪菌移植作为一种安全有效的治疗复发性艰难梭菌感染的方法已被广泛应用。在动物实验中,移植正常的粪便菌群可以改善中风的结果。
益生菌能够改善肠道菌群,调节细胞因子的释放,影响神经炎症反应,因此可能是急性中风的另一种治疗策略。动物研究表明,益生菌丁酸梭菌可以减轻脑缺血/再灌注造成的小鼠脑功能损伤。粪菌移植和益生菌干预还缺乏在脑中风患者中的临床研究,值得进一步的研究,它们或可作为降低中风的严重程度和促进中风后康复的有效手段。
饮食是影响肠道菌群组成的主要决定因素。事实上,饮食多样性与氧化三甲胺水平的变化也有关系,大量摄入含有左旋肉碱和磷脂酰胆碱的食物(比如红肉),可以增加肠道微生物产生的氧化三甲胺。高脂饮食会增加人体内氧化三甲胺的浓度,而地中海饮食会降低氧化三甲胺的产生。因此,控制饮食是一种改善中风的有效手段,一方面可以通过降低氧化三甲胺的产生而降低中风的风险,另一方面可以通过改善肠道菌群而改善中风结果和促进康复。

总结
肠道菌群与大脑之间存在着密切的相互作用,由于胃肠道并发症在中风患者中非常常见,所以肠道菌群在中风的发生和预后中的作用也日益受到关注。越来越多的研究发现,肠道菌群的改变可能是急性缺血性中风的一个危险因素,增加中风的发生风险;相反,中风也会导致肠道菌群的进一步紊乱,这可能会增加中风的严重程度,导致严重的胃肠道、肝、肾、心血管损伤,包括多器官功能障碍综合征,同时也会影响脑功能的恢复。改善肠道菌群,可能对于减少中风风险,降低中风后的严重程度以及改善预后具有重要意义。
图片均来自网络
参考文献:


编辑:田力




支付宝转账赞助
支付宝扫一扫赞助
微信转账赞助
微信扫一扫赞助